Forschung
Ziele
Die primären Ziele umfassen:
- Die strukturellen Merkmale von gesundem und bösartigem Gewebe mit 3D Biodruckern derart nachzubilden, dass sie die dreidimensionale Gewebearchitektur im menschlichen Körper möglichst realitätsnah wiedergeben. Im Gegensatz dazu sind aktuelle Standardmethoden, vor allem die zweidimensionale Kultivierung von Zellen auf Plastik, nur unzureichend in der Lage die physiologische Situation im Körper abzubilden.
- Testmodelle für patientenspezifische Arzneimitteltests zu entwickeln, um bei Behandlungsentscheidungen unterstützen, sowie langfristig Gewebeersatz- und Regenerationsstrategien zu entwickeln.
- Mithilfe unserer biogedruckten Gewebemodelle wollen wir Alternativen zu Tierversuchen anbieten um diese möglichst zu reduzieren bzw. langfristig zu ersetzen. Im Zuge dessen sind wir Partner des „MUI animalFree research cluster“ und Mitglied der RepRefRed Society. Weitere Infos dazu hier
Forschungsprojekte
Antonia Degen: 3D-biogedrucktes Gewebe zur Untersuchung von β-Oxidationsdefekten
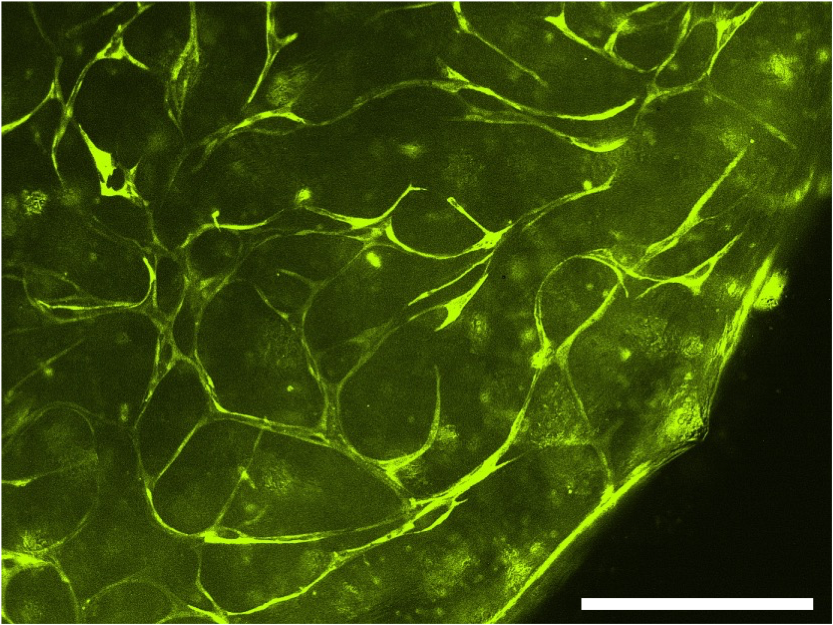
Im Rahmen der FG-15 Forschungsgruppe wird in diesem Projekt ein in vitro Modell zur Untersuchung genetisch bedingter Fettsäureoxidationsdefekte entwickelt (LCHAD-/VLCAD-Defekte). Dabei handelt es sich um vererbte Störungen der mitochondrialen Oxidation langkettiger Fettsäuren. Die 3D-biogedruckten Gewebestrukturen mit gesunden und defekten Patientenzellen ermöglichen die Untersuchung neuer Therapiemöglichkeiten und der Gewebereaktion unter physiologischer Belastung. Des Weiteren analysieren wir Defekte in der Mitochondrienstruktur der Patientenzellen und deren Restrukturierung. Da kardiologische Komplikationen bei LCHADD/VLCADD-Patienten häufig zu einer verkürzten Lebenserwartung führen, nutzen wir außerdem die Technologie der induzierten pluripotenten Stammzellen (iPSC). Dazu werden die Patientenzellen erst zu iPSCs reprogrammiert und anschließend zu Kardiomyozyten differenziert, um patientenabhängige Unterschiede und die Wirkung verschiedener Behandlungsmodalitäten zu untersuchen.
Alexeja Kleiter: Entwicklung eines 3D-biogedruckten Hautkrebsmodells
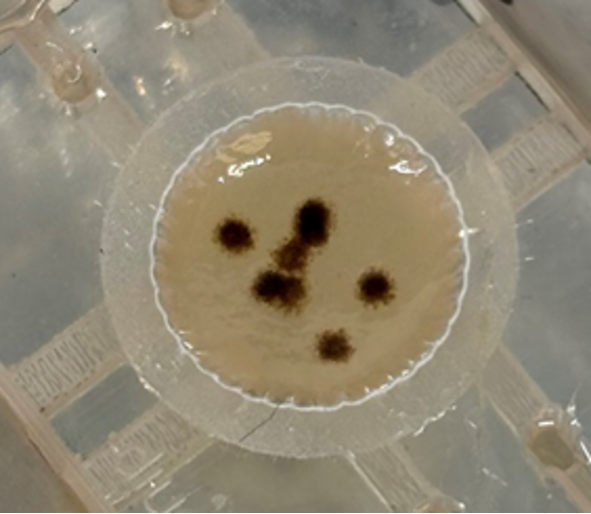
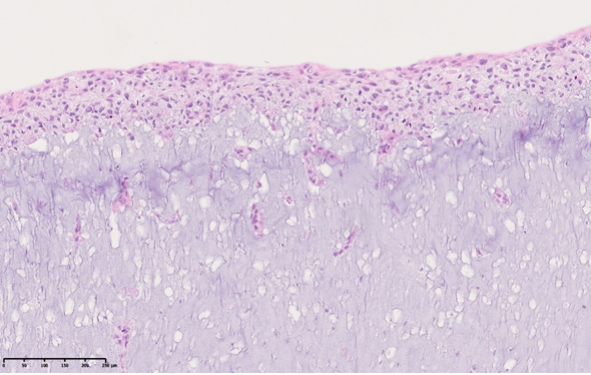
Das maligne Melanom ist eine der aggressivsten Formen von Hautkrebs und schwer zu behandeln. Um neue Therapieansätze zu entwickeln, ist es entscheidend, die Wechselwirkungen zwischen Tumorzellen und dem Immunsystem besser zu verstehen. Bisherige Forschungsmethoden basieren oft auf Tiermodellen, die nur begrenzt auf den Menschen übertragbar sind. Unser Ziel ist es daher, ein innovatives 3D-biogedrucktes Hautmodell zu etablieren, das die natürliche Tumorumgebung realistisch nachbildet. Dazu werden menschliche Fibroblasten und Keratinozyten in Mikro-Chips gedruckt und Melanom-Spheroide in das Modell integriert. In der Haut spielen dendritische Zellen (DC) und Langerhans-Zellen eine zentrale Rolle in der Immunabwehr und der Antitumor-Immunität. Tumorzellen nutzen jedoch Mechanismen, um deren Funktion zu unterdrücken. Um diese Prozesse genauer zu erforschen, differenzieren wir verschiedene DC-Subtypen und Langerhans-Zellen aus Stammzellen – ohne den Einsatz tierischer Zusätze. Durch die Kombination dieser Komponenten wollen wir die Wechselwirkungen zwischen Melanomzellen und Immunzellen in einem realistischen Hautmodell besser untersuchen. Dies ist besonders relevant für die Entwicklung innovativer Immuntherapien gegen das Melanom.
Entwicklung eines 3D-biogedruckten Neuroblastom-Modells mit Blutgefäßen zur Untersuchung der Metastasierung.
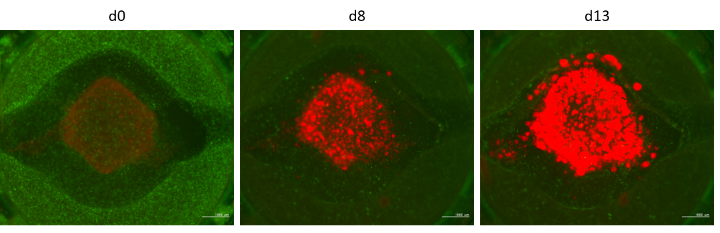
Das Fortschreiten des Neuroblastoms, eines hochmalignen Tumors der im Kindesalter auftritt, wird maßgeblich durch die Tumormikroumgebung und die Förderung der Blutgefäßbildung beeinflusst. Wir entwickeln ein 3D Biodruck Modell, um die Tumormikroumgebung des Neuroblastoms auf einem Fluidik-Chip zu rekonstruieren, indem wir Krebszellen mit Fibroblasten, Immunzellen und Blutgefäßen kombinieren. Dieser „Tumor-on-Chip“ wird mit anderen Gewebe-Surrogaten wie Leber und Niere in einem speziell entwickelten Perfusionssystem verbunden. Mithilfe dieser Screening-Plattform können gleichzeitig Aktivierung, Verstoffwechslung und Eliminierung von Medikamenten über Leber bzw. Nierenzellen, sowie deren Einfluss auf das Tumorwachstum bzw. Metastasierung untersucht werden. In diesem Projekt werden vor allem Modulatoren des Transkriptionsfaktors FOXO3 untersucht, der eine wichtige Rolle bei der Onkogenese und Chemoresistenz des Neuroblastoms spielt.
Verena Sturmlehner: Mesothelium-on-Chip Systems zur Untersuchung des Ovarialkarzinoms
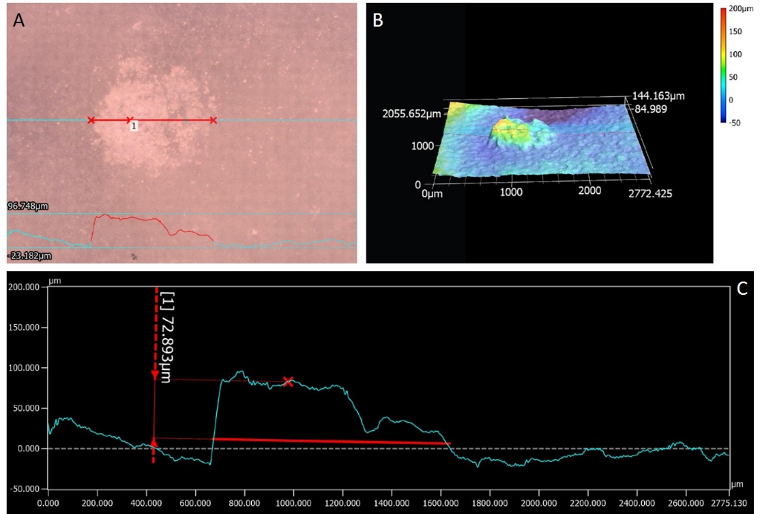
Das Ovarialkarzinom ist der tödlichste gynäkologische Krebs und die vierthäufigste Krebs-assoziierte Todesursache in der westlichen Welt. Ein Grund für die hohe Sterblichkeit sind multizelluläre Zellaggregate im Aszites bei mehr als 50% der Patientinnen, die mit Metastasierung ins Mesothel und Rezidivbildung assoziiert sind. Daher konzentrieren wir uns in diesem Projekt auf die Entwicklung eines Mesothel-on-Chip Modells, welches die Bildung von Blut- und Lymphgefäßen sowie mechanische Kräfte simuliert, um die Invasion der Ovarialkarzinom Zellaggregate ins Mesothel effizient nachzubilden. Dieses Model soll dazu beitragen das Ansprechen auf Standardtherapien auszutesten, sowie neue Medikamente zu erforschen.
Ersatz von Tierversuchen (3Rs: Replace-Reduce-Refine)
Uns ist der Ersatz und die Reduktion von Tierexperimenten ein grosses Anliegen. Mit unseren innovativen 3D Biodruck Modellen und menschlichen Tissue-on-Chip Modellen möchten wir diesbezüglich einen wichtigen Beitrag leisten und sind deshalb auch Partner im “MUI animalFree research cluster” an der Medizinischen Universität Innsbruck und Mitglied der RepRefRed Society.
Viele biomedizinische Fragestellungen und Therapien können nur im ganzen Organismus, d.h. im Versuchstier, getestet werden, bevor sie am Patienten Anwendung finden. Dem Tierversuch muss jedoch immer eine umfangreiche Analyse der zellbiologische Vorgänge und Medikamentenwirkung in Zellkulturen vorausgehen. Je besser die Zellkultur das natürliche Gewebe oder Tumorgewebe nachbildet, umso besser können diese in vitro Experimente auch auf das Versuchstier (bzw. den Patienten) übertragen werden. Auf diese Weise kann man Tierversuche deutlich reduzieren (reduce), einzusetzende Medikament-Konzentrationen präziser vorab einschätzen (refine) und im optimalen Fall Tierversuche vollständig ersetzen (replace).
Highlights
FFG/EFRE Infrastruktur Grant „2Photonen Polymerization 3D Druck Facility an der Medizinischen Universität Innsbruck“ (Projektleitung Judith Hagenbuchner, Michael Ausserlechner) – In Österreich einzigartiger Nanobiodrucker an der 3D Bioprinting Core Facility der MUI
MyPoint MUI, Projekte FFG
Start des MUI-finanzierten PhD Programmes CONNECT (Judith Hagenbuchner, Michael Ausserlechner)
MyPoint MUI
Daniel Nothdurfter erhält „Otto Seibert Preis“
MyPoint MUI
Michael Ausserlechner wird zum „Univ. Professor für Tissue Engineering“ an der Medizinischen Universität Innsbruck berufen
MyPoint MUI
Der „Staatspreis für Alternativen zum Tierversuch 2022“ wird von Bundesminister Martin Polaschek an Michael Ausserlechner verliehen
MyPoint MUI
Bioprinting Team an der MUI entwickelt einzigartiges 3D biogedrucktes, vaskularisiertes „Tumor-on-chip“ Modell zur personalisierten Medikamententestung
Biofabrication, MyPoint MUI, Tiroler Tageszeitung, Salzburger Nachrichten, STOL.IT, zm online, europe-cities.com, studium.at, ORF.at, openscience.or.at, Pflege-Professionell.at, medinlive.at, APA Science, Innovationorigins, Kleine Zeitung
Kiwanis Preis an Michael Ausserlechner Oktober 2022
Lienz: Tiroler Kiwanis Preis ging an Forscher aus Osttirol
Michael Ausserlechner erhält Forschungsförderung der Dr. Johannes und Herta Tuba Stiftung
MyPoint MUI
Judith Hagenbuchner entwickelt neues 3D Gewebemodell für die Erforschung genetischer Erkrankungen im Rahmen der FWF-geförderten Forschungsgruppe FG15
MyPoint MUI
Blog-Interview mit Michael Ausserlechner „Der Mensch aus dem 3D Drucker?“
medsolut.com
Interview von Judith Hagenbuchner mit eco.nova
eco.nova (Seite 74ff)
Judith Hagenbuchner erhält den Otto Seibert Wissenschaftspreis 2020
MyPoint MUI
Das Bundesministerium für Bildung, Wissenschaft und Forschung fördert innovatives 3D gedrucktes Tumor-on-Chip Projekt von Judith Hagenbuchner
MyPoint MUI